크립토코커스 수막염
기사의 의료 전문가
최근 리뷰 : 12.07.2025
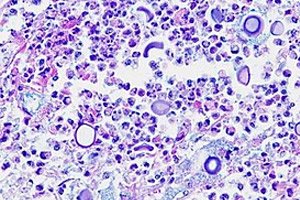
수막염은 박테리아, 바이러스, 원생생물뿐만 아니라 진균 감염에 의해서도 발생할 수 있습니다. 크립토코쿠스 수막염은 인간의 기회주의 병원균인 캡슐화된 효모 진균인 크립토코쿠스 네오포르만스(Cryptococcus neoformans)에 의해 발생합니다. [ 1 ] 1894년 오토 부세(Otto Busse)와 아브라함 부세케(Abraham Buschke)가 최초로 보고하여 부세-부세케병(Busse-Buschke disease)으로 명명되었습니다. [ 2 ]
ICD-10에 따르면, 질병 코드는 G02.1(중추 신경계의 염증성 질환에 관한 섹션)이고, 진균증(즉, 진균성 질환)에 관한 섹션에서는 B45.1입니다.
역학
암호코쿠스성 뇌수막염의 10건 중 8건은 HIV/AIDS에 감염된 사람에게서 발생합니다.
2017년 봄 랜싯 감염병(The Lancet Infectious Diseases)에 발표된 자료에 따르면, 이 곰팡이는 HIV 또는 AIDS 감염자에게 매년 약 22만 건의 크립토코쿠스 수막염을 유발하고, 그중 18만 명 이상이 사망합니다. 크립토코쿠스 수막염의 대부분은 사하라 이남 아프리카 지역에서 발생합니다.
WHO 통계에 따르면, 2017년에 아프리카에서 165.8만 건의 암호코쿠스 수막염 사례가 등록되었고, 아시아 국가에서 43.2만 건, 북미와 남미에서 9.7만 건, 유럽 국가에서 4.4만 건이 등록되었습니다.
원인 크립토코커스 수막염
영어: 이 유형의 수막염 의 원인은 Cryptococcus neoformans(Tremelomycetes강, Filobasidiella속) 진균 감염입니다.이 진균은 토양(먼지 포함), 썩은 나무, 새(비둘기)와 박쥐의 배설물 등 환경에 서식합니다.감염은 공기를 통해 발생합니다.진균의 에어로졸 담자포자를 흡입하는 것입니다.하지만 질병 발병에 대한 충분한 면역력이 있는 대부분의 사람들에게 C. neoformans는 감염을 일으키지 않고 통성 세포 내 기회주의 미생물(다른 사람을 감염시킬 수 없음)로 남아 있습니다.또한 읽어보세요 - Cryptococci - cryptococcosis의 원인균 [ 3 ]
일반적으로 암호코쿠스 수막염은 HIV 감염자(IVB 단계)에서 2차 감염으로 발생하며, 장기간 면역 억제를 동반한 다른 질병으로 인해 면역 체계가 제대로 작동하지 않는 사람에게서도 발생합니다. [ 4 ]
암호코쿠스 수막염은 호흡 기관과 폐에서 뇌와 척수로 C. neoformans가 혈행성으로 전파된 후 발생하는 암호코쿠스증의 뇌 또는 폐 외 형태로 간주됩니다.[ 5 ]
위험 요소
암호코쿠스 수막염 발병 위험을 증가시키는 요인은 다음과 같습니다.
- 신생아기(신생아기) 및 미숙아;
- 종양학 질환(백혈병, 다발성 흑색종, 림프육종 포함), HIV 감염 및 AIDS 환자 의 면역 체계 약화
- 당뇨병;
- 바이러스성 간염 및 기타 면역 복합 질환
- 낫적혈구빈혈
- 종양학적 진단이 있는 경우의 화학요법
- 허용 가능한 이온화 방사선 수준을 초과함
- 장기간의 항생제 또는 스테로이드 치료
- 혈관 내 카테터 및 션트 설치
- 골수나 내부 장기 이식.
병인
다당류 캡슐(식세포작용을 억제함)로 인간 면역 세포로부터 보호되는 암호포자충은 숙주 세포를 파괴할 수 있는 효소인 프로테아제, 우레아제, 인지질분해효소 및 뉴클레아제를 분비합니다. [ 6 ]
그리고 암호코코증의 발병 기전은 이들 효소가 세포막을 용해시키고, 분자를 변형시키고, 세포소기관의 기능을 방해하고, 세포골격을 변화시켜 세포를 손상시킨다는 사실에 있습니다. [ 7 ]
진균 세린 프로테아제는 세포 단백질의 펩타이드 결합을 파괴하고 면역 효과 세포의 면역글로불린과 단백질을 절단하며 C. neoformans 복제는 단핵 식세포(대식세포) 내에서 발생하여 확산을 촉진합니다. [ 8 ]
또한, 크립토코쿠스는 내피세포를 통과하고 감염된 대식세포 내로 이동함으로써 혈액-뇌 장벽(BBB)의 온전성을 파괴합니다. 이 진균은 혈류를 통해 뇌척수액으로, 그리고 뇌의 연막으로 퍼져 뇌 조직에 젤라틴성 가성낭(pseudocyst) 형태로 진균 세포 "군집"을 형성합니다. [ 9 ]
조짐 크립토코커스 수막염
암호코쿠스 수막염의 첫 징후는 발열(체온이 38.5~39°C로 상승)과 심한 두통입니다.
임상 증상에는 메스꺼움과 구토, 발작, 목의 경직, 눈의 빛에 대한 민감도 증가, 의식과 행동 장애 등이 포함됩니다. [ 10 ]
전문가들이 지적하듯, 수막증후군의 발병은 수막의 세균 감염보다 느립니다.
합병증 및 결과
암호코쿠스로 인한 진균성 수막염의 합병증 및 결과는 다음과 같습니다.
- 두개내압의 상당한 증가
- 안면 신경의 마비/부전을 동반한 두개 신경의 고립된 손상 및 시신경의 위축성 변화(안과적 문제로 이어짐)
- 염증 과정이 뇌의 피질하 조직과 반구 조직으로 확산되는 것 - 암호코쿠스성 수막뇌염
- 뇌농양(암세포종)의 발생
- 경막하 공간(뇌의 경막 아래)으로의 삼출액
- 척수 손상
- 정신적 변화와 인지 기능 저하.
감별 진단
감별 진단에는 세균성 및 바이러스성 뇌수막염 및 뇌수막뇌염, 진균 Histoplasma capsulatum, Coccidioides immitis, Blastomyces dermatidis 또는 아메바(Naegleria fowleri 포함)에 의한 뇌 손상이 포함됩니다.
치료 크립토코커스 수막염
병인학적 치료는 암호포자충을 근절하는 것을 목표로 하며, 이를 위해 항진균제를 사용합니다.
치료 요법에는 폴리엔계 항진균 항생제인 암포테리신 B(Amphocyl)를 정맥 내 투여(점적, 중심 정맥 카테터 또는 복막 주입)하고, 항진균제인 플루시토신(5-플루오로시토신) 또는 플루코나졸(살진균 및 항진균 효과가 있음)과 병용 투여하는 것이 포함됩니다. 이러한 약물의 용량은 환자의 체중에 따라 계산됩니다.
암포테리신 B는 신장에 독성 영향을 미치고 플루시토신의 부작용으로는 골수의 조혈 기능 억제, 호흡 또는 심장 마비, 표피 괴사증의 형태로 피부 병변이 발생하는 것 등이 있을 수 있으므로 환자의 상태를 지속적으로 모니터링하는 것이 필요합니다.
2010년 IDSA(미국감염학회) 업데이트에 발표된 권고 사항에 따르면, 치료는 10년 동안 변화가 없었습니다. 1차 항진균 치료는 다음 세 가지 유형의 환자에 대한 유도, 공고, 유지 요법을 기반으로 합니다. [ 12 ]
HIV 관련 질병
- 유도 요법
- 암포테리신 B 데옥시콜레이트(0.7-1.0mg/kg/일) + 플루시토신(100mg/kg/일 경구 투여) 2주간(증거 A1)
- 리포좀형 암포테리신 B(3-4mg/kg/일) 또는 지질 복합체 암포테리신 B(5mg/kg/일; 신장 기능 모니터링) + 플루시토신(100mg/kg/일)을 2주간 투여(근거 B2)
- 암포테리신 B 데옥시콜레이트(0.7~1.0mg/kg/일) 또는 리포좀형 암포테리신 B(3~4mg/kg/일) 또는 암포테리신 B 지질 복합체(플루시토신을 견딜 수 없는 환자의 경우 5mg/kg/일)를 4~6주 동안 투여(근거 B2)
- 유도 요법의 대안
- 암포테리신 B 데옥시콜레이트 + 플루코나졸(증거 B1)
- 플루코나졸 + 플루시토신 (증거 B2)
- 플루코나졸(증거 B2)
- 이트라코나졸(증거 C2)
- 플루코나졸(400mg/일) 8주간(자료 A1)
- 플루코나졸(200mg/일)을 1년 이상 복용(증거 A1)
- 이트라코나졸(400mg/일)을 1년 이상 복용(증거 C1)
- 암포테리신 B 데옥시콜레이트(1mg/kg/주)를 1년 이상 복용(증거 C1)
- 통합 치료
- 지지 치료
- 유지 관리 요법의 대안
이식 관련 질병
- 유도 요법
- 리포좀형 암포테리신 B(3-4mg/kg/일) 또는 지질 복합체 암포테리신 B(5mg/kg/일) + 플루시토신(100mg/kg/일)을 2주간 투여(근거 B3)
- 유도 요법의 대안
- 리포좀형 암포테리신 B(6mg/kg/일) 또는 지질 복합형 암포테리신 B(5mg/kg/일)를 4-6주 동안 투여(근거 B3)
- 암포테리신 B 데옥시콜레이트(0.7mg/kg/일) 4-6주간(증거 B3)
- 플루코나졸(400~800mg/일) 8주간 투여(증거 B3)
- 플루코나졸(200~400mg/일)을 6개월~1년 동안 복용(근거 B3)
- 통합 치료
- 지지 치료
비 HIV/이식 관련 질병
- 유도 요법
- 암포테리신 B 데옥시콜레이트(0.7~1.0mg/kg/일) + 플루시토신(100mg/kg/일)을 4주 이상 투여(근거 B2)
- 암포테리신 B 데옥시콜레이트(0.7–1.0 mg/kg/일)를 6주 동안 투여(증거 B2)
- 리포좀 암포테리신 B(3-4mg/kg/일) 또는 지질 복합 암포테리신 B(5mg/kg/일)를 플루시토신과 함께 4주간 투여(증거 B3)
- 암포테리신 B 데옥시콜레이트(0.7mg/kg/일) + 플루시토신(100mg/kg/일) 2주간 투여(근거 B2)
- 통합 치료
- 플루코나졸(400~800mg/일) 8주간 투여(증거 B3)
- 플루코나졸(200mg/일)을 6~12개월 동안 복용(근거 B3)
- 지지 치료
암포테리신 B와 플루시토신의 병용 요법은 감염 제거에 가장 효과적인 것으로 나타났으며, 암포테리신 단독 요법보다 생존율 향상 효과가 더 컸습니다. 그러나 플루시토신은 높은 가격으로 인해 자원이 부족하고 질병 부담이 높은 환경에서는 종종 구하기 어렵습니다. 암포테리신 B와 플루코나졸의 병용 요법이 연구되었으며, 암포테리신 B 단독 요법보다 우수한 결과를 보였습니다.[ 13 ], [ 14 ], [ 15 ]
치료하지 않으면 임상적 경과는 혼란, 발작, 의식 수준 저하, 혼수 상태로 진행됩니다.
진통제에 반응하지 않는 두통은 CT 또는 MRI를 이용한 적절한 신경영상 검사 후 척추 감압술로 치료할 수 있습니다. 1회 요추 천자로 배출할 수 있는 뇌척수액의 안전한 최대 용량은 명확하지 않지만, 10ml씩 배출할 때마다 압력을 확인하여 최대 30ml까지 배출하는 경우가 많습니다.[ 16 ]
예방
면역 체계가 약한 경우, 우선적으로 Cryptococcus neoformans 균 감염을 예방하는 것이 필요합니다.[ 17 ] 먼지가 많은 장소와 흙을 다루는 작업을 피하는 것이 좋으며, HIV 감염자는 지속적인 항레트로바이러스 치료를 받아야 합니다.
예보
치료를 하지 않으면 진균성 수막염의 예후는 좋지 않습니다.
초기 예후는 다음과 같은 사망률 예측 요인에 따라 달라집니다[ 18 ], [ 19 ]:
- 뇌척수액의 개방압력은 25 cm H2O 이상이다.
- 뇌척수액의 백혈구 수치가 낮음
- 감각 장애
- 늦은 진단
- 뇌척수액 항원 역가 상승
- 감염 제거율
- 뇌척수액의 효모 양은 10 mm3를 초과합니다 ( 브라질의 일반적인 관행)[ 20 ]
- 이미 언급된 것 외에도 HIV와 관련되지 않은 환자와 이들 환자의 예후 요인은 다음과 같습니다.
- 약한 염증 반응의 지표
- 두통 없음
- 원발성 혈액 악성종양
- 만성 신장 또는 간 질환
사망률은 자원 환경에 따라 국가마다 다릅니다. 미국과 프랑스에서는 10주차 사망률이 15%에서 26%로 여전히 높은 수준을 유지하고 있으며, HIV 비감염 환자의 경우 늦은 진단과 면역 반응 장애로 인해 더욱 높습니다. 반면, 자원이 부족한 국가에서는 늦은 내원과 약물, 혈압 모니터, 그리고 적절한 모니터링의 부족으로 인해 10주차 사망률이 30%에서 70%로 증가합니다.


