FDA, 빔젤엑스, 한선염 치료제로 승인
> 알렉세이 크리벤코, 의료 검토자
최근 리뷰 : 02.07.2025
최근 리뷰 : 02.07.2025
2024-11-26 14:17
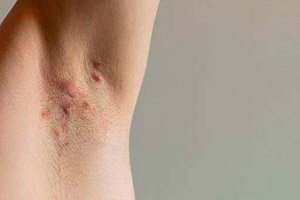 ">
">미국 식품의약국(FDA)은 중등도에서 중증의 히드라데니티스 화농증을 앓는 성인을 치료하기 위해 UCB의 빔젤스(Bimzelx, bimekizumab-bkzx)를 승인했습니다.
빔젤렉스는 인터루킨 17A(IL-17A)뿐만 아니라 인터루킨 17F(IL-17F)까지 선택적으로 억제하는 최초이자 유일하게 승인된 약물입니다. 이는 미국에서 빔젤렉스의 다섯 번째 적응증입니다.
승인 기준:
이 승인은 중등도에서 중증의 히드라데니티스 화농증을 앓고 있는 성인 환자를 대상으로 실시한 두 건의 3상 임상 시험(BE HEARD I 및 BE HEARD II)의 데이터를 기반으로 합니다.
핵심 성과 지표:
- HiSCR50: 16주차에 Bimzelx로 치료받은 환자 중 히드라데니티스 수푸라티바의 징후와 증상이 위약군에 비해 ≥50% 개선된 비율이 상당히 높았습니다(히드라데니티스 수푸라티바 임상 반응(HiSCR50) 점수로 측정).
2차 지표:
- HiSCR75: 이 약물은 위약과 비교했을 때 16주차에 ≥75% 개선(HiSCR75)을 달성한 환자에게 임상적으로 의미 있는 개선을 제공했습니다.
결과의 지속 가능성:
- 임상적 반응은 48주 동안 유지되었으며, 새로운 안전 신호는 확인되지 않았습니다.
전문가 의견:
보스턴에 있는 베스 이스라엘 디커니스 의료 센터의 BE HEARD 프로그램 연구원이자 피부과 의사인 알렉사 B. 킴볼 박사는
"중등도에서 중증의 히드라데니티스 화농증 치료에 Bimzelx를 승인한 것은 현재 충족되지 않은 임상적 요구가 크고 치료 옵션이 제한적인 상황에서 중요한 진전입니다."라고 말했습니다.

