조기 임신
기사의 의료 전문가
최근 리뷰 : 04.07.2025
지연 임신은 전통적으로 과학적으로나 실용적으로 큰 관심을 받는 문제 중 하나이며, 무엇보다도 이 병리로 인한 불리한 산전 결과로 인해 발생합니다.
국내 산부인과에서는 287~290일 이상 지속되는 만삭후 임신은 태아의 자궁 내 고통을 수반하며 생물학적 과숙 징후를 보이는 아이를 낳는 것으로 여겨지는데, 이는 산전/산중 고통 증후군이 발생할 위험이 높고 신생아 적응에 어려움을 초래합니다.
역학
임신 후기에 임신하는 경우는 전체 임신의 약 7%입니다(Martin et al., 2007).
미국산부인과학회(ACOG)는 임신 후기를 42주(294일) 이상 지속되는 임신으로 정의합니다. 발생률은 평균 약 10%입니다. 대부분의 유럽 국가에서는 임신 후기를 294일 이상 지속되는 임신으로 정의하지만, 포르투갈(287일 이상)과 아일랜드(292일 이상)는 예외입니다. 유럽에서 임신 후기의 발생률은 약 3.5~5.92%입니다.
동시에, 과숙 징후를 보이는 아이가 항상 과숙 상태로 태어나는 것은 아니며, 오히려 임신 290일 이전에 태어난 태아에게서 과숙 징후가 나타날 수 있는데, 이는 태아의 개별적인 시기와 임신 발달 특성 때문일 가능성이 높습니다. 그러나 태변 흡인 증후군, 중추신경계, 심근, 신장, 장의 저산소성 허혈 손상과 같은 심각한 합병증 발생 빈도가 높아 태아의 출생 전 및 출생 중 사망으로 이어질 수 있으므로, 과숙 태아의 기능적 상태에 더욱 주의를 기울여야 합니다.
만삭 임신은 출산 중 합병증의 빈도를 증가시키고 주산기 이환율과 사망률을 증가시키는 요인으로 간주됩니다. 만삭 임신의 가장 전형적인 주산기 합병증은 사산, 질식 및 출산 외상입니다. E. Ya. Karaganova, IA Oreshkova(2003)는 임신 주수에 따라 만삭 임신이 있는 499명의 환자에서 주산기 결과에 대한 철저한 분석을 수행한 결과, 임신 주수가 41주에서 43주로 증가함에 따라 주산기 이환율의 비율이 증가한다는 것을 발견했습니다. 따라서 임신 43주에서 저산소성 허혈성 중추신경계 손상의 빈도는 임신 주수가 41주 이하인 만삭 신생아에 비해 2.9배, 질식은 1.5배, 흡인 증후군은 2.3배 증가합니다. 임신 기간이 41주가 넘으면, 분만이 시작되기 전에 태아 고통의 징후가 태아의 67.1%에서 발견되었고(임신 기간이 42~43주인 태아의 절반에서 발견됨), 양수에 태변이 섞인 경우는 31.6%, 양수 과소증은 환자의 50.9%에서 발견되었습니다.
원인 조기 임신
지연 임신의 가장 흔한 원인은 부정확한 임신일 계산입니다(Neilson, 2000; Crowley, 2004). 분만 예정일(EDD)을 결정하는 데 표준 임상 기준을 사용하면 재태 연령을 과대평가하는 경향이 있어 지연 임신 발생률이 증가합니다(Gardosi et al., 1997; Taipale and Hiilermaa, 2001). 재태 연령을 확인하는 데 일반적으로 사용되는 임상 기준에는 마지막 월경 기간(LMP), 제1삼분기 양손 검진으로 평가한 자궁 크기, 태아 운동 감지, 태아 심음 청진, 그리고 자궁저부 높이 등이 있습니다. 단태 임신.
만삭이 지나 임신이 발생하는 경우, 그 원인은 일반적으로 알 수 없습니다.
위험 요소
신체적, 산부인과적 병력과 현재 임신의 특성을 분석하면, 지연 임신이나 장기 임신의 가능성을 시사하는 위험 요소가 발견됩니다.
임신 후기의 위험 요소:
- 임산부는 30세가 넘었습니다.
- 성병(STI) 및 자궁 부속기관의 만성 염증성 질환의 병력
- 배달이 늦은 적이 있다는 표시
- 임신 40주 이상이 지나도 자궁경부가 "미성숙"하거나 "충분히 성숙되지 않은" 상태입니다.
장기 임신의 위험 요소:
- 임산부의 연령은 20~30세입니다.
- 불규칙하거나 장기간(≥ 35일)의 월경 주기를 동반한 난소 기능 장애
- 마지막 월경 첫날을 기준으로 결정한 임신 주수와 초음파 검사 결과를 기준으로 결정한 임신 주수 사이의 불일치.
일반적인 위험 요인으로는 초산, 과거 임신 경험(Alfirevic 및 Walkinshaw, 1994; Mogren 등, 1999; Olesen 등, 1999), 남아 태아(Divon 등, 2002), 비만(Usha Kiran 등, 2005; Stotland 등, 2007), 호르몬 요인, 유전적 소인(Laursen 등, 2004) 등이 있습니다.
체질량지수(BMI)가 임신 기간과 분만 시기에 어떤 영향을 미치는지는 알려져 있지 않지만, 흥미롭게도 비만 여성은 만삭 임신을 경험할 가능성이 더 높고(Usha Kiran et al., 2005), BMI가 낮은 여성은 만삭 임신과 조산(임신 37주 이전에 분만) 위험이 더 높습니다(Hickey et al., 1997). 지방 조직은 호르몬 활성도가 높고(Baranova et al., 2006) 비만 여성은 대사 상태가 변화할 수 있으므로, 비만 여성에서 분만 시작과 관련된 내분비 요인이 변화했을 가능성이 있습니다.
유전적 요인은 임신 연장과 관련이 있을 수 있습니다. 만삭 이후 임신을 경험한 여성은 만삭 이후 임신 위험이 더 높습니다(상대 위험도 1.3)(Mogren et al., 1999). 이전에 만삭 이후 임신을 경험한 여성은 이후 만삭 이후 임신 위험이 더 높습니다(과거 만삭 이후 임신 경험이 한 번 있는 경우 27%, 두 번 이상 만삭 이후 임신 경험이 있는 경우 39%)(Kistka et al., 2007).
병인
만삭후 임신의 병인은 완전히 이해되지 않았습니다. 위에서 보여준 바와 같이, 만삭후 임신과 관련된 몇 가지 위험 요인이 몇 가지 가능한 설명과 함께 확인되었지만, 이 질환의 병인은 아직 명확하지 않습니다. 최근 몇 년 동안 분만에 대한 이해가 향상되었음에도 불구하고, 분만을 시작하고 진행을 촉진하는 정확한 기전에 대한 명확성이 여전히 부족합니다. 만삭후 임신의 병인을 더 잘 이해하려면 분만의 병태생리를 밝히고 이러한 기전이 만삭후 임신에서 촉발되지 않거나 반대로 조산에서 더 일찍 촉발되는 이유를 이해하려고 노력하는 것이 중요합니다. 이 세 가지 상태 사이에 실제로 공통된 기초 또는 관계가 있다는 것은 논리적으로 보입니다. 분만의 기전은 태반, 산모, 태아가 중요한 역할을 하는 호르몬, 기계적 및 염증 과정 간의 상호 작용을 포함합니다.
태반에서 부신피질자극호르몬 방출 펩타이드(CRH) 생성은 임신 기간과 관련이 있습니다(McLean et al., 1995). 태반 CRH 합성은 임신이 진행됨에 따라 기하급수적으로 증가하여 분만 시점에 정점에 도달합니다. 조산한 여성은 만삭 분만 여성보다 기하급수적으로 빠른 성장률을 보이는 반면, 만삭 분만 여성은 성장률이 더 느립니다(Ellis et al., 2002; Torricelli et al., 2006). 이러한 데이터는 만삭 이후 분만이 임신 기간을 조절하는 생물학적 기전의 변화로 인한 것임을 시사합니다. 이는 CRH와 분만을 연결하는 생리학적 경로의 유전자 다형성으로 인한 유전적 소인 때문일 수 있습니다. 또한, 비만 여성에서처럼 모체의 표현형이 분만 시 정상적인 호르몬 신호에 대한 모체 조직의 반응을 변화시킬 가능성도 있습니다.
CRH는 태아 부신을 직접 자극하여 태반 에스트리올 합성의 전구체인 DHEA를 생성할 수 있습니다(Smith et al., 1998). 모체 혈장 CRH 농도는 에스트리올 농도와 상관관계가 있습니다(Smith et al., 2009). CRH에 의해 유도된 에스트리올 증가는 임신 후반에 에스트라디올 수치보다 더 빠르게 증가하여 에스트리올 대 에스트라디올 비율이 증가하여 임신 마지막 몇 주 동안 에스트로겐적 환경을 조성하는 것으로 생각됩니다. 동시에 임신 중에 발생하는 모체 혈장 프로게스테론의 증가는 임신 후반에 느려지거나 심지어 감소합니다. 이는 CRH가 태반 프로게스테론 합성을 억제하기 때문일 수 있습니다(Yang et al., 2006). 따라서 에스트리올의 분만 촉진(자궁 수축 촉진) 효과가 증가함에 따라 프로게스테론의 임신 촉진(이완 촉진) 효과가 감소합니다. 이러한 비율 변화는 조산, 만삭 단태아, 그리고 쌍태아 임신에서 관찰되었습니다(Smith et al., 2009). 만삭 이후 임신의 상황은 알려져 있지 않습니다.
조짐 조기 임신
과숙 태아의 복합적인 증상은 발렌타인(1902)과 룽게(1948)에 의해 처음 기술되었으며, 이로 인해 발렌타인-룽게 증후군이라고 불립니다. 이 증후군은 치즈 같은 기름기가 없고, 신생아 피부(목욕 후 발, 손바닥)뿐만 아니라 사타구니와 겨드랑이 주름의 건조함과 짓무름, 긴 손톱, 두꺼운 두개골, 좁은 봉합선과 작은 크기의 천문, 피부, 태아막, 탯줄의 녹색 또는 황색 변색 등을 포함합니다. 다른 관찰 결과들은 임신 장기화를 시사합니다.
287일 이상 지속되는 장기 임신은 태아의 고통을 수반하지 않으며, 과숙의 징후 없이 건강한 아이를 출산하는 것으로 끝납니다. 따라서 장기 임신은 태아의 최종 성숙을 목표로 하는 생리적 상태로 간주됩니다.
합병증 및 결과
만삭 임신은 태아와 신생아의 이동성 및 이환율 증가와 산모 이환율 증가와 관련이 있습니다. 이러한 위험은 원래 생각했던 것보다 더 큽니다. 과거에는 두 가지 이유로 이러한 위험이 과소평가되었습니다. 첫째, 초음파가 임신을 정의하는 일반적인 방법이 되기 전에 만삭 임신에 대한 초기 연구가 발표되었습니다. 결과적으로 연구에 포함된 많은 임신이 실제로 만삭이 아니었습니다. 두 번째 이유는 사산 자체의 정의와 관련이 있습니다. 사산율은 전통적으로 진행 중인 (태아) 임신이 아닌 특정 재태 연령에 분만한 임신을 사용하여 계산되었습니다. 이는 만삭 임신의 사산율을 줄이는데, 태아가 분만되면 더 이상 자궁 내 태아 사망(IUFD)의 위험이 없기 때문입니다. 따라서 적절한 분모는 주어진 임신 주수에서의 모든 출산이 아니라, 진행 중인(태아가 아닌) 임신입니다(Rand et al., 2000; Smith, 2001; Caughey et al., 2003).
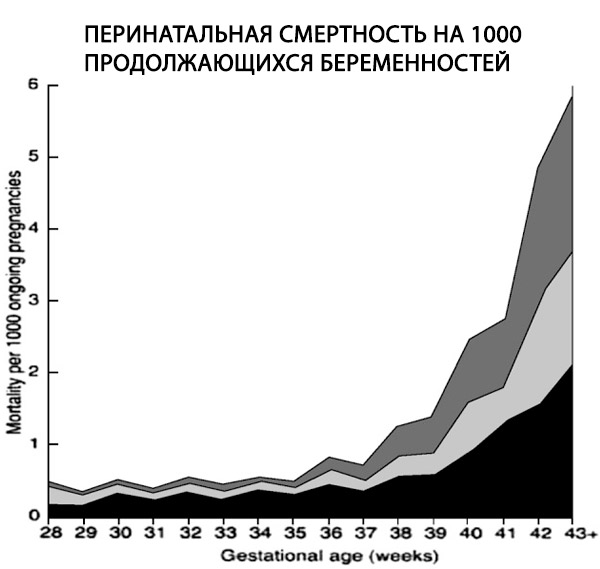
적절한 분모를 사용하여 17만 건 이상의 단태아 출산을 대상으로 한 한 회고적 연구에서는 1,000건의 임신 중 사산율이 0.35건에서 2.12건으로 6배 증가한 것으로 나타났습니다(Hilder et al., 1998).
태아와 신생아의 합병증
사산과 조기 신생아 사망으로 정의되는 주산기 사망률은 임신 42주에 만삭보다 두 배나 높습니다(출산 1,000건당 4~7건 대 2~3건). 43주에는 4배, 44주에는 5~7배 증가합니다(Bakketeig and Bergsjo, 1989; Feldman, 1992; Hilder et al., 1998; Cotzias et al., 1999). 또한, 이러한 자료는 임신 1,000건을 기준으로 계산할 때 태아 및 신생아 사망률이 임신 40주 이후에 급격히 증가함을 보여줍니다(Hilder et al., 1998)(Hilder et al., 1998).
자궁태반 기능 부전, 태변 흡인 및 자궁 내 감염은 이런 경우 주산기 사망률이 증가하는 주요 원인으로 여겨진다(Hannah, 1993).
태아 이환율은 만삭 임신과 임신 41주 이후 임신에서 증가합니다. 여기에는 태변 배출, 태변 흡인 증후군, 거대아, 그리고 성숙 장애가 포함됩니다. 만삭 임신은 또한 낮은 제대산도(신생아 산혈증), 낮은 5분 아프가 점수(Kitlinski et al., 2003), 신생아 뇌병증(Badawi et al., 1998), 그리고 생후 1년 이내 영아 사망률(Hilder et al., 1998; Cotzias et al., 1999; Rand et al., 2000)의 독립적인 위험 요인입니다. 이러한 영아 사망 중 일부는 태변 흡인 증후군과 같은 주산기 합병증의 결과인 것이 분명하지만, 대부분은 원인을 알 수 없습니다.
만삭 태아의 약 20%는 자궁태반 기능 부전으로 인한 만성 자궁내 성장 지연과 유사한 특징을 보이는 신생아를 지칭하는 난성 증후군을 앓고 있습니다(Vorherr, 1975; Mannino, 1988). 이러한 증후군에는 얇고 주름지고 각질이 일어나는 피부(과도한 각질), 마른 체형(영양실조), 긴 머리카락과 손톱, 양수과소증, 그리고 잦은 태변 배출이 포함됩니다. 이러한 임산부는 양수과소증, 태변 흡인, 그리고 저혈당증, 발작, 호흡 부전과 같은 단기 신생아 합병증으로 인해 탯줄 압박 위험이 증가합니다.
모성 위험
만삭 임신은 산모에게 상당한 위험을 초래합니다. 위험은 다음과 같이 증가합니다.
- 분만 장애(정기 분만 시 9-12% 대비 2-7%)
- 거대증과 관련된 심각한 회음부 상처(3도 및 4도 상처)(만삭아 3.3% 대 2.6%)
- 수술적 질 분만; 그리고
- 제왕절개(CS) 비율이 두 배로 증가(임신 말기 14% 대 7%)(Rand et al., 2000; Campbell et al., 1997; Alexander et al., 2000; Treger et al., 2002).
제왕절개술은 자궁내막염, 출혈, 혈전색전증의 발생률이 더 높은 것과 관련이 있습니다(Alexander et al., 2001; Eden et al., 1987).
신생아 예후와 마찬가지로, 산모 이환율 또한 임신 42주까지 만삭 임신과 함께 증가합니다. 융모양막염, 심각한 회음부 열상, 제왕절개, 산후 출혈, 자궁내막염과 같은 합병증은 임신 39주 이후에 증가합니다(Yoder 등, 2002; Caughey and Bishop, 2006; Heimstad 등, 2006; Caughey 등, 2007; Bruckner 등, 2008).
진단 조기 임신
만삭 임신의 전통적인 진단은 재태 연령을 정확하게 계산하는 것입니다. 동시에, 현 시점에서 가장 정확한 방법은 마지막 월경 첫날을 기준으로 한 계산과 임신 7주에서 20주까지의 초음파 검사 데이터를 기반으로 한 계산을 포함합니다. 많은 저자들은 이 두 가지 방법을 동등하다고 생각합니다. 그러나 일부 연구자들은 만삭 임신의 재태 연령을 결정할 때 초음파 생체 측정 데이터에만 의존할 것을 제안합니다. 만삭 임신의 위험 요인으로는 체세포, 산부인과적 병력, 그리고 현재 임신 과정의 여러 특징이 있습니다.
많은 저자들은 신체적 병력에서 부모의 연령이 30세 이상이고, 산모의 생식기 외 병리 존재를 강조합니다. 산부인과 병력의 특징 중 월경 장애, 유산 및 자연 유산의 존재, 자궁 부속기의 염증성 질환, 만삭 출산 병력, 그리고 3회 이상의 출산 임박 여부에 주의를 기울여야 합니다.
만삭후 임신의 실험실 진단
임신 기간이 길어짐에 따라 칼레크레인-키닌 시스템이 점진적으로 고갈되어 키니노겐 함량이 극도로 낮아지고(0.25–0.2μg/ml, N=0.5μg/ml), 칼레크레인과 그 억제제의 활동이 낮아지고, 임신 41주 이후에는 혈장의 자발적인 에스테라제 활동이 감소합니다.
만삭 임신에서는 임산부와 태아 모두에서 지질 과산화 과정이 심화되어 세포 내 구조의 막 결합 효소가 억제됩니다. 결과적으로 해독 및 에너지 생성 기능이 현저히 저하되고, 외인성 및 내인성 독성 대사산물이 축적되어 내독소혈증이 발생하며, 이는 임신 기간이 길어짐에 따라 진행됩니다. 내독소혈증의 강도는 적혈구의 흡착 능력과 중분자 단백질 농도로 평가할 수 있습니다. 과산화 및 내인성 중독의 증가는 태아 저산소증의 심각성과 상관관계가 있습니다.
만기 임신은 자궁내막과 자궁근층에서 합성되는 프로스타글란딘 F2α 함량이 낮은 것이 특징이며, 이는 분만 발달의 주요 조절 인자입니다.
임신 41주 이상에서는 혈장 점도, 요산 농도가 증가하고, 피브리노겐, 항트롬빈 III, 혈소판 수치가 감소하는 것이 관찰됩니다. 임신 41주 이상 여성의 자궁경부질 분비물에서 태아 피브로넥틴 농도가 5ng/ml 이상인 것은 신체가 분만에 대한 생물학적 준비가 잘 되어 있으며, 3일 이내에 자연적으로 진통이 시작됨을 나타냅니다. 이 방법의 민감도와 특이도는 각각 71%와 64%입니다.
임신 후기에 태아태반 복합체와 태아의 기능적 상태의 특징을 연구하는 것은 매우 중요합니다(초음파, 도플러 및 심박동 검사).초음파 검사 동안 태아 계측법을 시행하여 태아의 추정 체중을 결정하고 해부학적 발달을 평가합니다.12.2%의 사례에서 I–II도의 IUGR이 감지되었으며 이는 장기 임신에서 증후군이 감지되는 빈도와 크게 다르지 않습니다.동시에 80%의 사례에서 비대칭 형태의 IUGR을 감지했고 20%에서 대칭 형태를 감지했습니다.임신 후기는 뚜렷한 퇴행성 이영양증 변화(석화가 있는 GIII)의 초음파적 징후가 감지되는 것이 특징입니다.임신 후기 그룹에서 양수량 지수의 평균값은 7.25±1.48이었으며, 임신 후기에 일반적인 것은 양수량이 감소한 것입니다.
도플러 연구
주산기 결과를 예측하는 가장 중요한 요소는 임신 후기에 태아 혈역학적 장애의 단계를 결정하는 것입니다.
- 1기 - 태반 내 및 태아 태반 혈류 장애. 이 단계에서는 태아의 동맥 및 정맥 혈류 역학에 장애가 없습니다. 제대 동맥과 그 말단 분지, 그리고 나선 동맥의 혈관 저항이 증가합니다. 제대혈의 기체 조성 및 산-염기 평형 지표는 정상 범위 내에 있습니다.
- 2기 - 태아 혈액 순환이 집중화됨. 출생 시 신생아의 혈액에서 저산소증이 관찰됩니다. 이 단계에서는 두 가지 연속적인 단계로 구분됩니다.
- IIa - 태아 동맥 순환이 중앙화되고 정맥과 심장 내 혈류가 변하지 않는 초기 징후로, 다음과 같은 특징이 있습니다.
- MCA의 저항 감소(최대 50%까지) 또는 대동맥의 혈관 저항 증가
- CPC 감소(0.9로)
- 태아의 신동맥 저항이 정상의 25% 이하로 증가한다.
- IIb - 혈액 순환의 중등도 집중화와 정맥관 내 혈류 장애, 대동맥 판막의 혈류 속도 증가가 관찰됩니다. 이 단계에서는 다음과 같은 증상이 나타납니다.
- 대동맥의 혈관 저항이 동시에 증가하고 중대뇌동맥의 혈관 저항이 감소함
- CPC 감소
- 정맥관 내 평균 혈류 속도(Tamx)의 증가
- 대동맥 판막에서 평균 선형 혈류 속도와 체적 혈류 속도가 증가합니다.
- IIa - 태아 동맥 순환이 중앙화되고 정맥과 심장 내 혈류가 변하지 않는 초기 징후로, 다음과 같은 특징이 있습니다.
- 3기 - 태아 순환의 현저한 중심화와 정맥 유출 장애, 그리고 중심 및 심장 내 혈류역학의 대상부전. 출생 시 신생아의 제대혈에서 저산소증과 산증 및 고탄산혈증이 동반됩니다. 이 시기의 도플러 지표는 다음과 같은 특징을 보입니다.
- SMA의 혈관 저항이 정상의 50% 이상 감소, CPC가 0.8 이하로 감소
- 대동맥과 신동맥의 혈관 저항이 80% 이상 점진적으로 증가합니다.
- 정맥관에서 - S/A 비율, PIV(0.78 이상)의 증가 및 Tamx의 감소
- 하대정맥에서 PIV, IPI 및 %R이 증가(36.8% 이상)
- 경정맥에서 S/A 비율, PIV(1.1 이상)가 증가하고 Tamx가 감소합니다.
- 대동맥과 폐동맥 판막의 평균 선형 속도와 체적 속도가 감소함
- 심박수 증가, 박출량 감소, 좌심실 최종 수축기 및 최종 이완기 용적, 심박출량 감소.
확인된 태아 혈역학 변화 단계는 만삭 임신 중 만성 자궁내 저산소증 하에서 태아의 기능적 상태 장애가 지속적으로 진행됨을 반영합니다. 신생아의 제대혈에서 저산소증과 고산혈증 및 고탄산혈증이 함께 검출될 경우, 단독 저산소증 환자군에 비해 주산기 합병증 발생 빈도가 4.8배 더 높습니다. 결과적으로, 고산혈증과 고탄산혈증은 만삭 임신 중 만성 저산소증 하에서 태아의 대사 장애가 심화되고 상태가 점진적으로 악화됨을 반영합니다.
심박조영술
1기에서 이 방법을 시행할 경우, 만성 자궁 내 저산소증(20.93%)과 중등도 태아 저산소증(6.97%)의 초기 징후가 관찰되었습니다. 2a기에서는 태아 저산소증 초기 징후 빈도가 2배 증가했고, 중등도 저산소증은 4.13배 증가했습니다. 2b기에서는 중등도 및 중증 태아 저산소증 빈도가 유의미하게 증가했습니다. 3기에서는 중증(65.1%)과 중등도(30.2%)의 태아 저산소증만 관찰되었습니다.
임산부 선별검사 프로그램은 다음과 같습니다.
- 임신 후기 임신 위험이 있는 임산부 식별
- 신생아 성숙 징후를 평가하는 초음파 태아 측정법
- 양수의 양과 질 평가
- 태반의 성숙도 평가
- 심박조영술;
- 태아 혈역학(중대뇌동맥, 대동맥, 정맥관, 하대정맥) 평가
- 태아의 생물학적 프로필 평가
- 자궁경부 성숙도 평가
- 양수검사.
검사하는 방법?
감별 진단
장기 임신 중인 여성을 종합적으로 검사하면 다음과 같은 사실이 드러납니다.
- 관찰 결과의 26.5%에서 2등급, 51.8%에서 3등급 태반 성숙;
- 관찰 결과의 72.3%에서 양수의 양은 정상이었습니다.
- 관찰 결과의 89.2%에서 태아-태반 혈류 지표가 정상이었고, 91.6%에서 뇌-태반 비율이 정상이었습니다.
- 100%의 관찰 결과 - 태아의 중심 혈류역학, 판막을 통한 혈류 및 정맥 혈류가 정상적으로 나타납니다.
- 태아-태반 및 태아 혈류 지표가 정상이면서 CPC가 감소한 것은 태아의 기능적 상태에 이상이 있음을 나타내며 IUGR, 자궁 내 감염 및 만성 태아 저산소증의 특징입니다.
누구에게 연락해야합니까?
치료 조기 임신
정확한 임신 날짜 계산은 만삭 임신의 진단 및 관리에 매우 중요합니다(Mandruzzato et al., 2010). 전통적으로 마지막 생리 주기를 사용하여 예상 분만일(EDD)을 계산해 왔습니다. 그러나 생리 주기 불규칙, 최근 호르몬 피임법 사용, 또는 임신 초기 출혈 등으로 인해 많은 부정확성이 발생할 수 있습니다.
임신을 위한 정기 초음파 검사를 실시하면 양성으로 진단되는 위양성률이 낮아지고, 전반적인 임신 후기 비율을 10~15%에서 약 2~5%로 줄일 수 있으며, 불필요한 개입을 최소화할 수 있습니다(Bennett et al., 2004; Caughey et al., 2008a; 2009).
임신 후기 임신 치료의 목표는 다음과 같습니다: 태아 혈역학적 장애 교정, 분만 중 태아 진행 방지, 분만을 위한 산도 준비, 분만 유도.
입원에 대한 지표
임신 기간이 40주 3일을 넘었고, 출산 예정일이 정확하게 계산되었으며, 지연 임신에 대한 위험 요소가 존재하고, 산도가 제대로 준비되지 않은 경우입니다.
임신 후기 임신의 약물 치료
임신 후기에 태아의 상태를 교정하기 위해 헤소벤딘 + 에타미반 + 에토필린(인스테논)이라는 약물이 사용됩니다. 이 약물은 각 성분의 효과가 상호 증강되어 신경 보호 효과가 있는 복합 약물입니다.
헤소벤딘 + 에타미반 + 에토필린 약물 투여에 대한 적응증:
- 태아의 태반동맥의 혈류 장애(SDO > 2.7, IR > 0.65)
- 뇌태반계수 감소(CPC < 1.10)
- 태아 순환의 중앙화의 초기 징후
- CTG 자료에 따르면 태아 저산소증의 초기 징후가 나타납니다. 태아 곤란증의 초기 징후를 나타내는 나열된 요인들은 응급 분만을 필요로 하지 않지만, 분만 중 태아 뇌의 적응 능력을 향상시켜 저산소증을 교정해야 할 필요성을 시사합니다.
임신 후기 출산 준비
자궁경부 자극의 기계적 방법:
- 태아 방광 아랫부분 박리. 태아 방광 아랫부분 박리는 프로스타글란딘 합성 증가 및 자궁경부 "숙성"을 유발할 수도 있습니다. 매일 또는 일주일에 2~3회 시행하는 태아 방광 아랫부분 박리는 자궁경부의 분만 준비 및 분만 유도에 도움이 됩니다. 이 방법은 매우 효과적이고 시행하기 쉬우며 부작용 발생 빈도가 낮고 비용도 저렴합니다. 단점으로는 진찰 중 임산부가 느끼는 불편함, 드물게 발생하는 출혈, 태아막 파열 가능성이 있습니다.
- 자궁경부 풍선 확장술. 자궁경부 풍선 확장술에는 폴리 풍선 카테터가 사용됩니다. 카테터를 자궁경관에 삽입하고 팽창시킵니다. 이 방법은 자궁경관을 기계적으로 확장하고 프로스타글란딘 합성을 촉진합니다. 카테터를 통해 양막 외 공간으로 생리식염수를 주입하여 자궁 하부를 확장하고 진통을 촉진할 수 있습니다.
- 천연 및 합성 원료의 기계적 확장기. 분만을 위해 자궁경부를 준비하기 위해 천연 원료인 라미나리아(laminaria)와 합성 원료인 딜라판(dilapan), 기판(gipan), 라미셀(lamicel)의 자궁경부 확장기를 사용합니다. 이 확장기는 직경 2~4mm, 길이 60~65mm의 탐침입니다. 라미나리아는 해조류인 라미나리아 자포니쿰(Laminaria japonicum)의 천연 재료로 만들어집니다. 합성 확장기는 흡습성이 좋은 화학적 및 생물학적으로 불활성인 중합체로 만들어집니다. 탐침-확장기는 필요한 양만큼 자궁경부관에 삽입됩니다. 흡습성으로 인해 자궁경부관에 있는 액체를 흡수하고, 크게 팽창하여 자궁경부에 요골 압력을 가합니다. 또한 자궁경부를 기계적으로 열어 분만 시작을 촉진합니다. 합성 자궁경부관 확장기는 불편함을 유발하지 않으며 환자가 잘 견딥니다. 합성 확장기는 자궁경관에 오래 머물러 상행 감염 위험을 증가시키므로 제한적으로 사용하는 것이 중요합니다. 자궁경부에 작용하는 기계적 방법은 자궁경부에서 내인성 프로스타글란딘 E2 합성 반응을 유발하여 자궁경부 구조 내 콜라겐의 양을 감소시키고 불안정화시켜 평활근을 이완시키는 효과를 나타냅니다. 또한, 프로스타글란딘 E2는 분만 초기에 우세하게 나타나는 것으로 알려져 있습니다.
약
프로스타글란딘 E2 계열의 제제가 사용됩니다. 실제 산부인과에서 검증된 가장 일반적인 분만 준비 및 유도 방법은 프로스타글란딘 E2 제제입니다. 프로스타글란딘 E2는 자궁경부 내 투여용 젤, 질정, 페서리 등 다양한 제형으로 제공됩니다. 프로스타글란딘 E2의 자궁경부 숙성 및 분만 시작 효과는 80~83%에 달합니다. 그러나 프로스타글란딘 E2를 사용하면 협응되지 않는 격렬한 분만과 정상 위치에 있는 태반의 조기 박리가 발생할 수 있습니다. 따라서 프로스타글란딘 E2는 태아 심장 활동 및 자궁 수축력에 대한 심박동도 검사를 의무적으로 시행하는 산부인과 병원에서만 투여해야 합니다.
환자 교육
반드시:
- 여성들에게 임신 주수와 예산일을 정확하게 계산할 수 있는 능력을 보장하기 위해 월경 주기를 기록하도록 교육하고, 태아의 운동 활동이 감소하거나 증가할 때 태아 저산소증 위험을 신속하게 판단하기 위해 태아의 움직임을 세는 것.
- 임신 기간이 40주 3일을 넘은 경우 태아의 상태를 철저히 평가해야 할 필요성과, 불리한 예후 요인이 있는 경우 입원이 필요할 수 있음을 환자에게 알립니다.
추가 관리
임신 기간이 40주를 초과하는 여성의 검사 및 관리에 대한 표준:
- 만삭 이후 임신과 장기 임신의 감별 진단을 실시합니다.
다음과 같은 경우에는 임신 후기 임신을 고려해야 합니다. 30세가 넘은 임산부의 첫 출산이 예정되어 있고, 월경 주기가 규칙적이며, 자궁 부속기의 성병 및 만성 염증성 질환의 병력이 있고, 출산이 늦은 징후가 있고, 마지막 월경 첫날과 임신 7~20주 사이에 실시한 초음파 검사 데이터를 기준으로 계산한 임신 주수를 준수하고, "미성숙" 또는 "불충분하게 성숙"된 자궁 경부가 있는 경우, 초음파 검사에서 GIII기 태반 성숙도 또는 양수 과소증이 발견되는 경우입니다.
장기 임신은 다음과 같은 경우에 나타납니다. 임산부의 나이가 20~30세인 경우; 난소 기능 장애로 인해 불규칙하거나 길어진(35일 이상) 월경 주기를 보이는 경우; 마지막 월경 첫날을 기준으로 한 임신 주수와 초음파 검사에서 나타난 임신 주수 사이의 불일치; "성숙한" 자궁 경부가 발견된 경우; 초음파 검사에서 태반이 GI 및 GIII 수준으로 성숙하고 돌화가 없으며 양수량이 정상인 경우.
- 태아의 상태를 정확하게 평가하고, 부정적인 산전 결과를 예방하기 위해, 임신 기간이 40주를 넘는 모든 임산부는 태아의 동맥 혈류 역학을 조사하는 도플러 초음파 검사를 받아야 합니다.
- 태아 혈역학에 변화가 없다면, 에스트로겐을 투여하고, 동적 CTG 조절과 함께 프로스타글란딘 E2 젤을 자궁경부에 매일 투여하고, 태아 혈류 상태를 모니터링(3일마다)하여 출산을 준비합니다.
- 혈액 순환의 집중화가 감지되면 정맥 혈류와 심장 내 혈역학을 검사하여 태아의 보상 능력을 파악하고 분만 방법과 시기를 선택합니다.
- 임신 후기에는 태아 혈역학이 단계적으로 변화합니다.
1기 - 태반 내 및 태아 태반 혈류 장애. 이 단계에서는 태아의 동맥 및 정맥 혈류 역학에 장애가 없습니다. 제대 동맥과 그 말단 분지, 그리고 나선 동맥에서 혈관 저항이 증가함을 알 수 있습니다. 제대혈의 기체 조성 및 산-염기 상태 지표는 정상 범위 내에 있습니다.
2기 - 태아 순환의 집중화. 출생 시 신생아의 혈액에서 저산소증이 관찰됩니다. 이 단계에서는 두 가지 연속적인 단계를 구분해야 합니다.
- IIa - 정맥과 심장 내 혈류가 변하지 않은 태아 동맥 순환의 중앙화 초기 징후
- IIb - 정맥관의 혈류가 손상되고 대동맥 판막의 혈류 속도가 증가하면서 혈액 순환이 약간 심하게 집중됩니다.
3기 - 태아 순환의 현저한 중앙화와 정맥 유출 장애, 그리고 중심 및 심장 내 혈류역학의 대상부전. 출생 시 신생아의 제대혈에서 산증 및 고탄산혈증을 동반한 저산소혈증이 관찰됨.
- CPC가 감소(< 1.1), 태아 혈역학의 집중화(초기 집중화: MCA의 SDO < 2.80; Ao > 8.00)와 정맥관의 평균 혈류 속도의 증가(중등도 집중화: MCA의 SDO < 2.80; Ao > 8.00; VP의 Tamx > 32cm/s), CTG 데이터에 따른 태아 저산소증의 초기 징후가 감지되면 태아 뇌의 적응 능력을 증가시키기 위한 산전 준비 측면에서 헤소벤딘 + 에타미반 + 에토필린을 정맥 투여하는 것이 표시됩니다.
- 초기 중심화(중대동맥 SDO < 2.80; 또는 태아 대동맥 SDO > 8.00)의 경우, 신체의 분만 생물학적 준비가 양호하고, 합병증이 없는 산부인과 병력이 있으며, 평균 태아 크기이고, 태아 심혈관계의 세심한 심장 모니터링 하에 양막절개술 후 자연 산도를 통한 계획 분만이 가능합니다. 신체의 분만 생물학적 준비 부족, 악화된 산부인과 병력, 그리고 태아의 크기가 큰 경우 계획된 제왕절개술을 통한 분만이 필요합니다.
- 태아의 모든 보상 기전의 긴장과 분만을 위한 예비 능력의 부족으로 인해 태아 혈역학의 중등도의 중앙 집중화가 나타나는 경우(MCA의 SDO < 2.80, 대동맥의 SDO > 8.00; VP의 Tamx > 32cm/s)에는 계획된 기준으로 제왕절개 분만이 표시됩니다.
- CTG 데이터에 따르면 태아 혈류의 동맥과 정맥 통로 모두에서 장애가 감지되고(현저한 중앙화: MCA의 SDO < 2.80 및 대동맥 > 8.00; VPr의 S/A > 2.25, PIV > 1.00; IVC의 %R > 16%, PIV > 1.2) 중등도 또는 중증 태아 저산소증이 동반된 경우 태아 혈역학의 대상 상실을 나타내므로 응급 제왕절개술을 통한 분만이 필요합니다.
예방
- 산전 관리를 받는 여성들 사이에서 임신 후기 위험군을 파악합니다.
- 태반 기능 부전 및 거대 태아의 예방.
- 마지막 생리일(생리 주기가 규칙적이었던 날)과 임신 20주 전에 실시한 초음파 검사를 고려하여 임신 기간과 생년월일을 신중하게 계산합니다.
- 출산을 위해 산도를 준비하고 태아의 상태를 평가하기 위해 임산부를 적절한 시기에 입원시키는 것입니다.



 [
[